
| Главная |
| Поиск по сайту |
Адрес этой страницы' ?>
<<Предыдущая страница Оглавление книги Следующая страница>>
Глава 14
ПОКРЫТИЯ РУТЕНИЕМ, РОДИЕМ, ПАЛЛАДИЕМ И ИХ СПЛАВАМИ
Гальванопокрытия рутением
Рутений применяют в качестве гальванопокрытия для электрических контактов, работающих в условиях эрозионного износа. При повышенных температурах покрытия не тускнеют и не теряют блеска на воздухе и в среде, богатой кислородом. Это позволяет их использовать для защиты серебра от потемнения (толщина 1-1,5 мкм) при изготовлении отражателей. По износо- и коррозионной стойкости рутениевые покрытия (толщина 1—2 мкм) сопоставимы с родиевыми. Цвет рутениевых покрытий серебристо-белый. Их твердость достигает 1200 кгс/мм2, а износостойкость примерно в 10 раз выше, чем серебряных. Удельное электросопротивление рутениевых покрытий составляет 14,5 х х 10-4 Ом•м.
Наиболее применимым для получения таких покрытий является хлоридный электролит (в г/л):
Хлорид рутения (RuCl3) 2-3,5 НСl 35-40
Режим электролиза: температура электролита 20 ± 5 °С, iк = 40 ÷ 50 А/дм2, ток переменный, Sк:Sа=3:1 (iа=17 А/дм2). Направление тока изменяют с помощью диодов, включенных в рабочую сеть в противоположных направлениях. Реостаты последовательно соединяют с диодами, что дает возможность подобрать любые соотношения iк:iа.
Покрытия по меди, латуни, серебру, платине получаются светлыми, но матовыми, толщина их < 15 мкм, твердость 900-1100 кгс/мм2. Для уменьшения потерь металла при электролизе в связи с образованием летучей и ядовитой четырехокиси рутения катодное и анодное пространство ванны разделяют диафрагмой. При рутенировании применяют нерастворимые аноды из платины.
Наряду с хлоридным применяют нитрозохлоридный электролит, содержащий RuNOCl3 (в виде металла) (4 — 5 г/л) и H2SO4 (5-15 г/л). Режим электролиза: температура электролита 65-70 °С iк = 1,0÷1,5 А/дм2, аноды -из платины. Покрытия толщиной до 6 мкм при таких условиях получаются светлыми и плотными.
В сернокислом (сульфаматном) электролите рутений существует в трех- и четырехвалентной форме, а в нитрозо-хлоридном — только в четырехвалентной. После катодной проработки содержание четырехвалентного рутения во всех электролитах уменьшается. При анодной проработке форма рутения не изменяется. Зависимость ηк от катодной плотности тока в нитрозохлоридном электролите представлена на рис. 62.
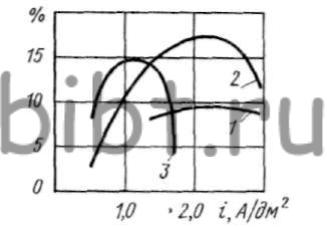
Рис. 62. Зависимость выхода по току от плотности тока в электролите:
1-6,5 г/л RuNOCl3 и 16 г/л H2SO4 (анод без диафрагмы); 2 — тот же, с диафрагмой; 3-3 г/л Ru и 110 г/л H2SO4
Для уменьшения внутренних напряжений в электролит рекомендуется вводить Al2(SO4)3, а ηа повышать за счет добавки трилона Б (30 — 50 г/л). В сернокислом электролите, содержащем гидрооксихлорид рутения (4 г/л) и H2SO4 (150 г/л), цвет покрытий изменяется в зависимости от содержания в нем серной кислоты: при заниженном они получаются темными, а при повышенном — светлыми и полублестящими.
Предварительное серебрение или палладирование латуней позволяет избежать их подтравливания в процессе рутенирования. На платиновом аноде при рутенировании наблюдается выделение кислорода, а при iа = 0,4 А/дм2 — образование бурых паров RuO4.
Наиболее перспективным электролитом является нитрозосульфаминовый (в г/л):
Нитрозохлорид рутения (металл) 4-5
Сульфаминовая кислота 50 — 60
Режим электролиза: температура электролита 60 —70°С, iк = 1,0 А/дм2, рН = 1,5 — 2,0, аноды — из платины.
Катодный выход по току достигает 100 % при рН = 2,0, при дальнейшем повышении рН покрытия темнеют. При перемешивании электролита уменьшается ηк. Покрытия рутением толщиной < 2,5 мкм гладкие и блестящие с 55 — 65%-ной отражательной способностью. Микротвердость таких покрытий составляет 800-900 кгс/мм2.
Трудность получения растворимых соединений рутения препятствует широкому внедрению этих покрытий. Однако под действием переменного тока рутений легко растворяется в разбавленных минеральных кислотах. Так, растворение порошкообразного рутения ведут (при его контакте с платиновой проволокой) при iк = 0,1 А/дм2 в растворе соляной кислоты. В результате получается раствор четырех-хлористого рутения, обеспечивающий катодное восстановление плотных компактных покрытий, надежно сцепленных с основой и с ηк ~ 12%. Разность потенциала между платиной и порошком рутения составляет 0,148 В. При этом рутений выполняет функцию анода. Платиновая проволока той частью, которая находится в рутениевом порошке, должна быть изолирована кислотостойким лаком.