
| Главная |
| Поиск по сайту |
Адрес этой страницы' ?>
<<Предыдущая страница Оглавление книги Следующая страница>>
ПОКРЫТИЯ РОДИЕМ
Микроструктура покрытия родием.
Гальванопокрытия родием.
Родиевые покрытия отличаются большой твердостью (до 900 кгс/мм2), обусловленной высоким значением активационного перенапряжения и содержанием соосаждаемого водорода. Покрытия обладают мелкозернистой структурой. Отражательная способность их в среде сероводорода и других сернистых соединений может превышать отражательную способность серебра и золота (рис. 63). Покрытия не растрескиваются и характер основы не влияет на значения напряжений. При кипячении в воде внутренние напряжения снижаются.
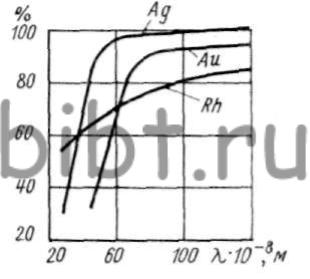
Рис. 63. Зависимость отражательной способности от длины волны
Родиевые покрытия не окисляются при t < 500°C, что обеспечивает стабильность их переходного сопротивления. Тонкий слой родия используют как барьер, предотвращающий диффузию между золотом и медью, серебром и пермаллоем. Покрытия родием молибденовых и вольфрамовых деталей снижают их электронную эмиссию.
В большинстве случаев родий осаждают из сульфатных электролитов. Их преимущества перед фосфатными и аминохлоридными: большая стабильность и возможность получения толстых слоев родия. Сульфатный электролит содержит Rh (5 ÷7 г/л) и H2SO4 (40 ÷ 50 г/л). Температура электролита 20-30°С, iк = 0,8÷1 А/дм2. Добавление в электролит 5 — 6 г/л алюминия или магния способствует почти полному снятию напряжений в осадках. Примеси (добавки) серебра и висмута в электролите повышают отражательную способность покрытий. Детали следует подвешивать под током, а в процессе родирования встряхивать их. Такие условия электролиза обеспечивают ηк = 70÷75% при iк = 0,8 А/дм2.
При уменьшении концентрации родия в электролите на 10% ухудшается качество покрытия, поэтому электролит следует корректировать из расчета убыли и только концентрированным раствором сульфата родия. Содержание H2SO4 необходимо поддерживать в пределах 45 — 50 г/л. Добавки сульфамата натрия и селеновой кислоты снижают внутренние напряжения родиевых покрытий. С повышением температуры от 25 до 50°С ηк увеличивается от 40 до 60%, а при перемешивании и прочих равных условиях электролиза — до 90%. Зависимость ηк от iк и температуры электролита показана на рис. 64 — 65.
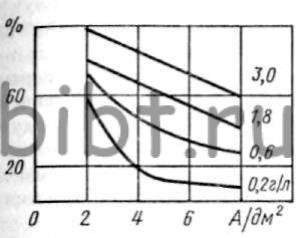
Рис. 64. Зависимость выхода по току от плотности тока при различной концентрации родия в электролите (содержание H2SO4 равно 26 г/л; температура электролита 50°С)
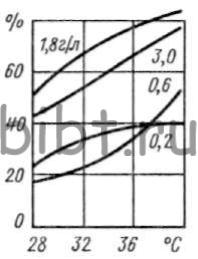
Рис. 65. Зависимость выхода по току от температуры при различной концентрации родия в электролите
Кривые изменения катодного потенциала (рис. 66) от iк имеют два резко отличающихся друг от друга участка: первый характерен значительной поляризацией при малых значениях iк, а второй — крутым подъемом поляризационных кривых. При малых значениях iк определяющим является диффузионный процесс, а при больших значениях iк — химическая поляризация. Повышение концентрации H2SO4 приводит к некоторому снижению предельной плотности тока, а увеличение концентрации родия в электролите — к ее повышению.
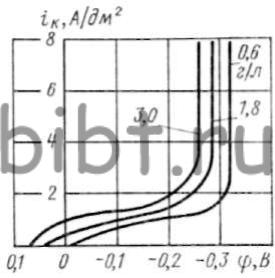
Рис. 66. Кривые катодной поляризации родия (H2SO4 = 50 г/л) при различной его концентрации в электролите
В процессе родирования вследствие высокой агрессивности электролита происходит подтравливание деталей и накопление меди, цинка, железа и других металлов в растворе, что приводит к получению губчатых и темных покрытий. Допустимая концентрация этих металлов не превышает 2 — 3 мг/л. Примеси цианидов и щелочных соединений в электролите родирования вызывают пассивацию отдельных участков катода.
Родиевые покрытия не защищают мерные металлы и легкие сплавы от коррозии, поэтому для них требуется комплекс промежуточных покрытий цинковое, медное, никелевое). Серебро можно родировать, однако на покрытии возможны разводы и белые пятна, появляющиеся за счет трещин в тонких слоях. Эти дефекты не устраняются даже полировкой. Поэтому серебро следует предварительно протравить в 50%-ном растворе H2SO4 и нанести слой никеля толщиной 10 мкм.
Процесс родирования следует вести в стеклянной ванне, так как контакт электролита с органическими материалами приводит к тому, что покрытия родия становятся черными, а выход по току сильно уменьшается. Серые и темные покрытия получают при пониженной концентрации родия и загрязнении электролитов примесями. Когда детали перед покрытием плохо обезжиривают и активируют, осадки на катоде становятся пятнистыми.
Аминохлоридный электролит родирования содержит аминохлоридную соль [Rh(NH3)5Cl]Cl2 концентрацией Rh3+ (6—7 г/л) в виде металла. Для получения 1 л электролита 25 г RhCl3•4H2O растворяют в 100 мл дистиллированной воды, нагретой до 40 —50°С и при энергичном перемешивании обрабатывают 25%-ным раствором аммиака. Затем эту смесь нагревают на водяной бане при 90 —95°С до перехода осадка в аммиачный комплекс и удаления избытка аммиака.
Реакция образования комплекса: RhCl3 + 5NH4OH = [Rh(NH3)5Cl]Cl2 + 5Н2O.
В полученный раствор добавляют горячую дистиллированную воду, корректируют рН в пределах 7,5 — 8,5 и приступают к работе. Режим электролиза: температура электролита 70 — 80 °С, iк = 2÷4 А/дм2, ηк = 57÷65%, аноды - из листового родия по ГОСТ 13098-67 (99,7% родия и 0,3% благородных металлов), постоянное перемешивание электролита и периодическая фильтрация. В результате получают светлое блестящее покрытие микротвердостью 800 — 850 кгс/мм2, Микроструктура родиевого покрытия представлена на рис. 67.

Рис. 67. Микроструктура покрытия родием из электролита при iк = 0,6 А/дм2 (х400)
При низкой концентрации Rh3+ и высоких значениях рН аминохлоридного электролита получают темные покрытия. Белый налет и полосы на покрытии появляются под влиянием низких значений iк или высокой температуры. Блестящие покрытия с низким значением ηк осаждаются при малых значениях рН и малой концентрации Rh3+. Примеси железа и никеля в электролите вызывают образование налета и шелушение покрытия.
Регенерацию и очистку электролитов родирования ведут посредством осаждения родия на медную фольгу с последующим ее растворением в азотной кислоте, также поступают и с бракованными деталями. Затем мелкие чешуйки родия промывают, сушат и измельчают в ступе. Порошок, смешанный с перекисью бария, масса которого в 3 раза больше, спекают в фарфоровом тигле при 900 °С (в течение 4 ч), обрабатывают соляной кислотой, упаривают до удаления избытка НСl, разбавляют водой и удаляют из раствора соли бария добавлением H2SO4 по каплям. Полученный раствор RhCl3 используют для приготовления электролита.
Регенерацию родия из промывных вод ванн-уловителей производят путем доведения рН до 7 и выпаривания воды до получения раствора соли типа Rh(OH)3.
От примесей различных металлов электролит очищают экстракционным способом с помощью диэтилдитиокарбамата натрия. При рН =3 этот экстракт-агент образует комплексное соединение серебра, ртути, свинца, меди и других металлов.
Родий не образует комплексы с этим агентом и остается в электролите в неизменном виде. Поэтому к очищаемому электролиту добавляют 20%-ный раствор этого вещества в четырех-хлористом углероде при рН = 3. Раствор тщательно перемешивают в течение 3 — 5 мин.
Для освобождения электролита от органических примесей его обрабатывают активированным углем или кипятят, добавив 30%-ный раствор Н2O2 (10 — 15 мл/л) с последующей фильтрацией. Если электролит загрязнен ионами С1-, то родий осаждают в виде гидроокиси, вводя в ванну 30%-ный раствор КОН. Выпавший осадок при этом отмывают от хлора и используют для приготовления свежего электролита.