
| Главная |
| Поиск по сайту |
Адрес этой страницы' ?>
<<Предыдущая страница Оглавление книги Следующая страница>>
ПОКРЫТИЯ СУРЬМОЙ
Гальванопокрытия сурьмой
Гальванопокрытия сурьмой используют для частичной замены оловянных при изготовлении печатных схем для обеспечения надежной пайки, для замены кадмия при защите стальных изделий от коррозии в морских условиях и др. Цвет покрытий серебристый блестящий.
Для осаждения сурьмяных покрытий применяют электролит (в г/л):
Сурьмяновиннокислый калий 50 — 70
Сегнетова соль 3 — 5
Соляная кислота (1,19), мл/л 3 — 5
Формалин, мл/л 0,5—1,0
Режим электролиза: температура электролита 20 ± 5°С, рН = 1,75 ÷ 1,9, iк=0,5 ÷1,0 А/дм2, ηк = 95 ÷ 98% и ηа = 100% (рН корректируют добавлением соляной кислоты). Электролит требует предварительной проработки в течение 10 — 20 ч при iк = 0,25 А/дм2 и Sa:Sк = 4:1. При этом можно получать качественные покрытия сурьмой толщиной до 200 мкм. Такие покрытия представляют интерес и для создания омических и выпрямляющих контактов на полупроводниках.
Процесс выделения сурьмы на катоде лимитируется кристаллизационной поляризацией, как и висмута, так как оба металла имеют электронное состояние s2p3, и их кристаллические решетки определяются значительной ковалентной составляющей связи.
В тартратных растворах сурьмяные аноды легко пассивируются. Добавка сегнетовой соли способствует растворению пассивной пленки. Скорость растворения сурьмы (рис. 60, участок 1) не зависит от концентрации тартрат-ионов. Потенциал анодного растворения не изменяется и при замене тартратов цитратами.
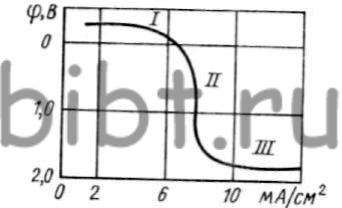
Рис. 60. Кривые анодной поляризации сурьмы в тартратном электролите (рН = 1,8)
Максимум перенапряжения анодного растворения Sb соответствует рН = 5 (0,15 В). Это связано с нарастанием концентрационной поляризации по ионам Н+, так как растворение сурьмы происходит по реакции
Sb + Н2O - 3ē -> SbO+ + 2Н+. Тартрат-ион играет основную роль в последующем образовании комплекса с ионами сурьмы, которое происходит даже в прианодном слое по реакции:
SbO+ + [tart]2- -> [SbO(tarl)]-.
Поэтому комплексообразование сурьмы является определяющим фактором при переходе от участка I к участку II. При недостатке тартрат-ионов у поверхности анода повышается концентрация ионов SbO+, что приводит к образованию малорастворимой трех-окиси сурьмы. При равенстве скоростей образования и растворении пассивной пленки скорость анодного процесса не зависит от потенциала.
Для получения качественных сурьмяных покрытий применяют электролиты (в г/л):
Сульфатно-щелочной
Na2S 60-65
NaOH 25-30
Na2CO3 35-40
Sb (в виде металла) 50 — 60 Солянокислый
НСl 100-110
Sb (в виде металла) 60-65
Водно-глицериновый NaOH 105-110
Sb (в виде металла) 20 - 25
Глицерин, мл/л 60 - 70
В первом электролите имеет место равновесие:
SbS-2 + S2- -><- SbS3-3
и на катоде первичным процессом является восстановление комплексных дитиоантимонит-ионов. Последние восстанавливаются при отсутствии ионов SbS-2, и разряд их сопровождается выделением водорода.
В водно-глицериновом электролите при наличии щелочи сурьма содержится в виде комплексных анионов типа SbS-2 и SbS3-3. В солянокислом электролите катодное восстановление протекает с участием анионов SbCl4-или SbCl3-6.
Осадки сурьмы из сульфатно-щелочного электролита получаются аморфно-кристаллическими, из водно-глицериновых — кристаллическими, а из солянокислых — аморфными. Микротвердость сурьмяных покрытий в основном составляет 115 — 120 кгс/мм2. На рис. 61 представлена зависимость ηк и коэффициента отражения сурьмяных покрытий от iк в сульфатном электролите.
![Зависимость выхода но току (1) и коэффициента отражения (2) покрытия от плотности тока [1,5 г/л (Sb2SO4)3, 150 г/л H2SO4]](1-107.jpg)
Рис. 61. Зависимость выхода но току (1) и коэффициента отражения (2) покрытия от плотности тока [1,5 г/л (Sb2SO4)3, 150 г/л H2SO4]
Для скоростного осаждения сурьмы на полупроводники применяют электролит, который приготовляют следующим образом: 370 г металлической сурьмы растирают в ступке, просеивают через сито, помещают в фарфоровую чашку и заливают серной кислотой (1,84) в количестве 8 — 17 г.
Смесь подогревают при непрерывном перемешивании до прекращения выделения SO2-4 и образования однородной белой массы тестообразной консистенции. После этого в рабочую ванну из винипласта наливают 440 — 450 мл 40%-ной фтористоводородной кислоты и постепенно при перемешивании вводят полученную массу. Затем смесь разбавляют, вводя в нее 370 мл дистиллированной воды, тщательно перемешивают и отстаивают в течение нескольких суток. Готовый электролит требует проработки при 20 ± 5 °С в течение 70 — 100 ч при iк = 50 А/дм2 с анодами из сурьмы. Режим электролиза: температура 15 —25 °С, iк = 30÷50 А/дм2, ηк=ηа=100%.