
| Главная |
| Поиск по сайту |
Адрес этой страницы' ?>
<<Предыдущая страница Оглавление книги Следующая страница>>
§ 2. КРИСТАЛЛИЧЕСКОЕ СТРОЕНИЕ МЕТАЛЛОВ И СПЛАВОВ
Основным признаком кристаллических тел является их внутреннее строение.
Изучение внутреннего строения металлов и сплавов при помощи рентгеновского анализа позволило ученым сделать вывод, что причины изменения свойств металлов и сплавов заключаются в том, что мельчайшие частицы -атомы, из которых они состоят, в различных условиях приобретают иное взаимное расположение. Атом состоит из положительно заряженного ядра и окружающих ядро отрицательно заряженных электронов.
Атом в целом электрически нейтрален, т. е. не обладает электрическим зарядом. Электроны движутся вокруг ядра с огромной скоростью. Атом бывает в таких состояниях, когда он приобретает или теряет электроны. Тогда он становится электрически заряженным -превращается в ион.
При избытке электронов ион является отрицательно заряженным, а при недостатке электронов -положительно заряженным,
Металлы состоят из положительно заряженных ионов и свободных, т. е. оторвавшихся от ядер, электронов, которые переходят от одних ионов к другим и вращаются вокруг ядра то одного иона, то другого. То или иное расположение атомов, из которых состоят металлы, называется их внутренним строением или структурой.
Отличительной особенностью кристаллических тел является то, что составляющие их атомы расположены в строго определенном порядке и образуют так называемую пространственную кристаллическую решетку.
Тела, в которых атомы расположены хаотически, т. е. в беспорядке, называются аморфными. К ним относятся: клей, пластмассы, стекло и др. От расположения атомов в кристаллической решетке зависят свойства металла.
Кристаллические решетки в металлах могут быть разных типов. Примеры таких кристаллических решеток изображены на рис. 2.
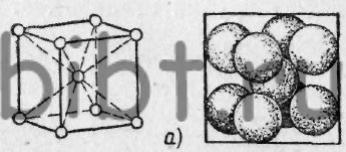
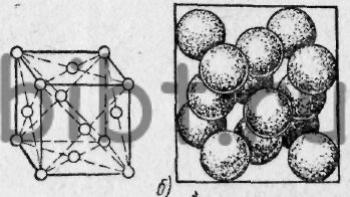
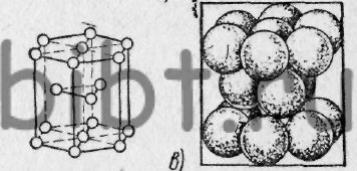
Рис. 2. Типы кристаллических решеток:
а - объемноцентрированный куб - атомы (ионы) металла расположены в вершинах куба, а один атом (ион) - в центре его, б - гранецентрированный куб - атомы (ионы) металла расположены в вершинах куба и в центре каждой из его граней, в - гексагональная решетка - 12 атомов расположены в вершинах шестигранной призмы, 2 -в центре оснований и 3 -в среднем сечении
Каждому из металлов свойственно то или другое кристаллическое строение. Например, железо в холодном состоянии состоит из ячеек 1-го типа, медь -из ячеек 2-го типа, цинк - из ячеек 3-го типа и т. п.