
| Главная |
| Поиск по сайту |
Адрес этой страницы' ?>
<<Предыдущая страница Оглавление книги Следующая страница>>
КАТОДНОЕ ВОССТАНОВЛЕНИЕ ПРОСТЫХ И КОМПЛЕКСНЫХ ИОНОВ
Схема движения гидратированного иона и его разряда на катоде.
Катодное восстановление простых и комплексных ионов
Ионы в электролите окружены оболочкой из молекул воды, которая состоит из облакообразной сферы дипольных молекул Н2O
Первый слой гидратной оболочки, например катионов, в большинстве случаев составляет четыре или шесть молекул воды, связанных с ионом парой свободных ионов. Следовательно ближайшие молекулы воды присоединены к катионам координационными связями и в этом отношении практически не отличаются от других аддентов, образующих комплексные ионы. Другие слои дипольных молекул гидратной оболочки ионов связаны с последними электростатически.
В массе раствора М (рис. 6 см. ниже) ионы мигрируют под действием относительно слабых электрических полей, деформация их гидратных оболочек А сравнительно небольшая. От катионов отстают или деформируются те молекулы воды, которые составляют диффузионную часть гидратной оболочки. При входе катиона в диффузионный слой Д, градиент потенциалов которого выше, чем массы раствора, деформация гидратной оболочки доходит до первого слоя Б молекул. Приближаясь к двойному электрическому слою Э, градиент потенциала возрастает настолько, что из диффузионной части гидратной оболочки отрываются почти все молекулы воды, за исключением первого гидратного слоя, который в сильно деформированном виде сохраняется до следующей ступени катодной реакции В.
Молекулы первого гидратационного слоя воды, связанные с катионами семиполярными или координационными связями, отрываются от последних в двойном электрическом слое Э(Г), градиент потенциала которого высокий. Дегидратация ионов от последних молекул воды требует затрат энергии - это энергия активации. Она проявляется ростом перенапряжения, называемого химической поляризацией.
Катодное восстановление металлов из комплексных ионов, например,
![]()
или
![]()
сводится к непосредственному разряду на катоде комплексных ионов. При разрядке комплексных ионов с отрывом от них аддентов на катоде создаются совершенно другие условия по сравнению с разрядом обычных гидратированных ионов.
Во-первых, комплексные соединения с небольшим числом аддентов часто бывают малорастворимыми. Поэтому при постоянном отрыве аддентов от центральных ионов создаются условия для образования в прикатодном слое коллоидов, которые оседают на поверхность катода и затрудняют диффузию адсорбируемых атомов разряжающего металла на поверхности катода. Во-вторых, комплексные электролиты, как правило, являются сильнощелочными и содержат относительно большой избыток ионов ОН-. Эти гидроокиси, особенно в прикатодном слое, могут конденсироваться с образованием мелкозернистой фазы. Частицы этой фазы, попадая на поверхность катода, способны еще больше усиливать катодную пленку и затруднять процесс электрокристаллизации.
Таким образом, при электрокристаллизации металлов из щелочных комплексов на катоде могут образоваться как пассивные пленки, состоящие из малорастворимых комплексных соединений с более низким числом аддентов, так и пленки смешанного состава, содержащие комплексные соединения и гидроокиси или окислы осаждаемых металлов.
На электрокристаллизацию и ее характер в щелочных комплексных электролитах значительное влияние оказывает сильная химическая адсорбция ионов или молекул аддентов, например CN-, NH3 и др.
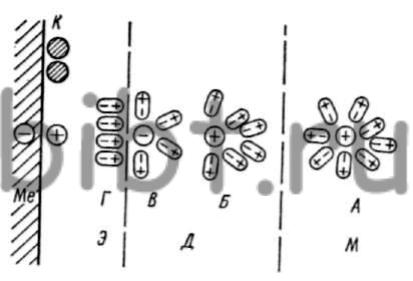
Рис. 6. Схема движения гидратированного иона и его разряда на катоде:
М - масса раствора; Д - диффузионный слой; Э - двойной электродный слой; К - центр кристаллизации; Me - металл катода